F بزرگی نیروی عمودی وارد بر سطح بر حسب نیوتون
A سطحی که نیرو بر آن وارد شده بر حسب متر مربع
P فشار بر حسب نیوتو بر متر مربع یا پاسکال
واحد فشار درSI نیوتون بر متر مربع است که پاسکال هم نامیده می شود. یک پاسکال معادل فشاری است که یک نیروی یک نیوتونی بر سطح یک متر مربع وارد می کند. هر قدر نیروی عمودی وارد بر سطح افزایش یابد و یا سطح تماس کاهش یابد بر مقدار فشار افزوده می شود. (و بر عکس)
به نکات زیر توجه کنید :
اگر می خواید فقط جزواتی را دانلود کنید که برای مدرسه است و هیچ محتوای اضافه تری ندارد باید مطالبی را دانلود کنید که متن روبرو را در سرتیترخود دارند
جزوات مدرسه
بقیه جزوات نکته هایی دارند که سر بعضی کلاس ها گفته شده و یا هم که مهم اند و در بعضی از آزمون های شنبه ها اومده و بعضی دیگه را هم از منابع دیگه گلچین کردیم...
این پــــست و پــــست بعدی ثابت است برای دانلود جزوات و نمونه سوالات وخدمات بیشتر به پایین بروید
شما می تونید جزوات و نمونه سوالات و هر چیز دیگه را به آدرس ایمیل mmadshahbazi@gmail.com و یا arya.aliakbari@gmail.com تا با اسم خودتون اون را انتشار بدیم اگه واقعا عالی و تقریبا کامل به درد بخور بود می زاریم تو سایت ...
سلام برسون
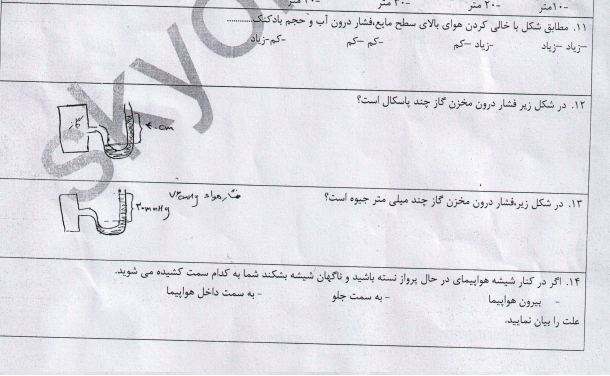
جزوات مدرسه
(زیست نهم (همه
حجم: 4.83 مگابایت
همه جروه زیست نهم امسال از طبقه بندی تا الان هرچی آقای حائری گفته نه بیشتر نه کمتر...
جزوات مدرسهنکات مهم شیمی:
جزوات مدرسه
هشتایی شدن تعداد الکترونهای موجود در بیرونی ترین لایه الکترونی (لایه ظرفیت)و دستیابی به آرایش الکترونی گازهای نجیب مبنایی برای سنجش پایداری اتم ها و در واقع میزان واکنشپذیری آنهاست. انجام شدیدترین واکنش ها آنهایی هستند که طی آنها اتم ها به این آرایش هشتایی پایدار دست مییابند. وقتی اتمی به آرایش هشتایی پایدار میرسد، از واکنشپذیری آن کاسته میشود و دیگر تمایلی به تشکیل پیوندهای بیشتر، از خود نشان نمیدهد. پس،اتمی که در لایه آخر خود کمتر از هشت الکترون دارد واکنشپذیر است، زیرا میتواند برای رسیدن به آرایش هشتایی پایدار، با اتمهای دیگر به مبادلۀ الکترون بپردازد. اکنون آرایش الکترونی اتمهای کلر، آرگون و پتاسیم را درنظر بگیرید. تفاوت آرایش الکترونی اتم واکنشپذیر پتاسیم تنها به علت وجود این تک الکترون در لایه ظرفیت آن است، زیرا با از دست دادن این الکترون ذره ای به دست می آید که آرایش الکترونی آن با آرایش الکترونی پایدار اتم آرگون (گاز نجیب پیش ازآن) یکسان خواهد بود.
برای مشاهده بقیه مطلب بروی ادامه مطلب کلیک کن
جزوات مدرسه
روند تغییر شعاع اتمی در جدول تناوبی:
بیشتر فضای اتم خالی است. در واقع الکترونها در محدودههایی حرکت میکنند که شبیه به ابر به نظر میرسند. با این تشبیه میتوان تصور کرد که تا چه اندازه، اندازهگیری ابعاد اتمها دشوار است، زیرا مرزهای یک تودۀ ابر مانند، نامشخص و متغیر است. اندازۀ یک اتم به وسیلۀ شعاع آن تعیین میشود. بنا بر تعریف به نصف فاصلۀ میان هستۀ دو اتم مشابه در یک مولکول دو اتمی شعاع اتمی گفته میشود. بر اساس این تعریف تعیین شعاع برخی از اتمها در شکل 6 نشان داده شده است. در روش دیگری برای تعیین شعاع اتمها از اندازهگیری فاصلۀ بین اتمی در بلور یک عنصر استفاده میشود. به دلیل همین تنوع در روشهای تعیین شعاعهای اتمی جدولهای مربوط به این مقادیر معمولاً با یک دیگر اندکی تفاوت دارند. توجه داشته باشید که در شکل 6 اتمها به صورت گویهای سادهای تصور شدهاند. آیا تغییر شعاع اتمی عنصرها از یک روند تناوبی برخوردار است؟ در شکل 7 شعاع اتمی عنصرهای گروههای اصلی آمده است. به نظر شماشعاع اتمی عنصرها در هر گروه از جدول تناوبی چگونه تغییر میکند؟ اگر به آرایش الکترونی عنصرهای جدول توجه کنیم متوجه میشویم که با حرکت از باال به پایین در یک گروه جدول به ازای هر تناوب یک لایه الکترونی جدید به تعداد لایه های الکترونی عنصرها افزوده میشود. بنابراین، شعاع اتمی به دو دلیل در یک گروه از عنصرها افزایش مییابد: آ( با زیادشدن لایه های الکترونی، شعاع اتمی نیز افزایش مییابد. به عبارت دیگر، الکترونها در فاصلههای دورتری نسبت به هسته قرار میگیرند.
بقیه روند ها در ادامه مطلب